
專家視角丨藥物研發過程中的化學對照品探討
精準藥物分析的工作,離不開穩定的分析系統和可靠的標準物質(標準品/對照品等)。標準物質具有復現、保存和傳遞量值的基本作用,對實現測量結果的溯源性,保證測量結果在時間與空間上的連續性與可比性,進而確保測量結果的準確可靠、有效與國際互認具有關鍵作用。
島津為制藥行業客戶提供穩定可靠的標準品/對照品制備解決方案:制備液相系統(Prep LC)、質譜引導的制備液相系統(MS-trigger Prep LC),超快速制備純化液相色譜系統(UFPLC)、制備超臨界流體色譜(Prep SFC)。

超快速制備純化液相色譜系統(UFPLC)可在線完成從分離、濃縮、純化到回收的制備全過程。
2020年,中國藥科大學藥物分析系吳春勇博士于新藥仿藥CMC實操討論群進行了精彩而全面的主題分享,并發表在“新藥仿藥CMC實操討論”公眾號,經過“新藥仿藥CMC實操討論”的授權,在此分享吳春勇博士的《化學藥物研發過程中的對照物探討》。
概述





相關要求及對照品來源




案例
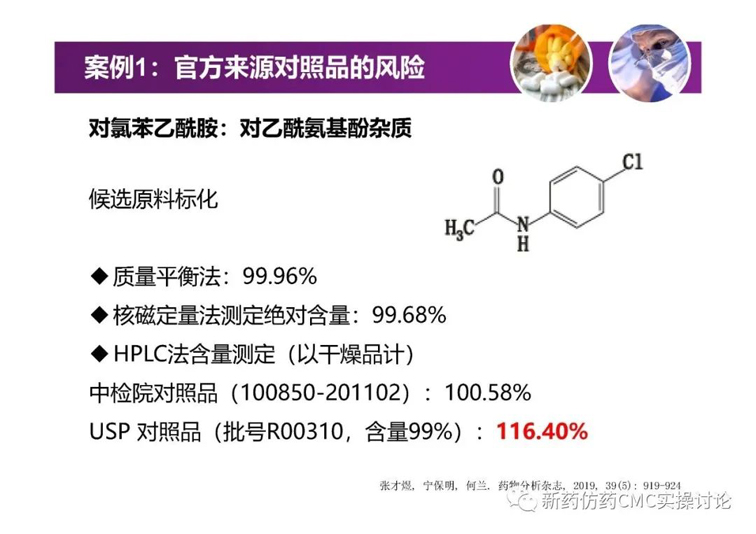

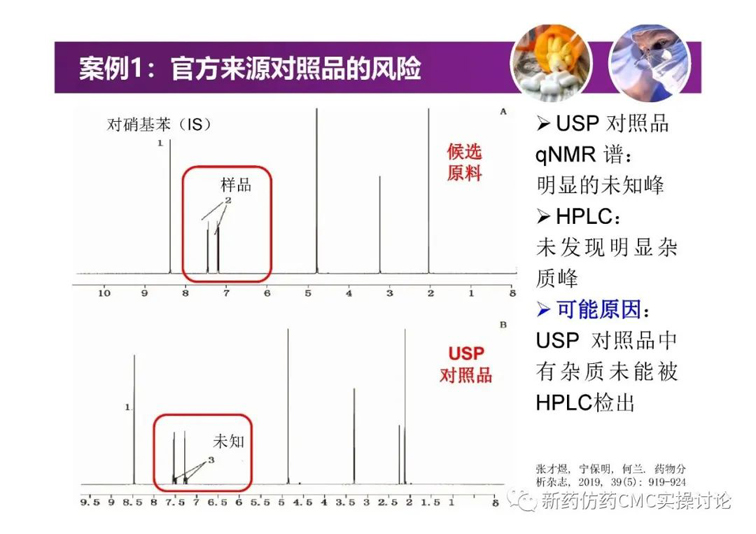

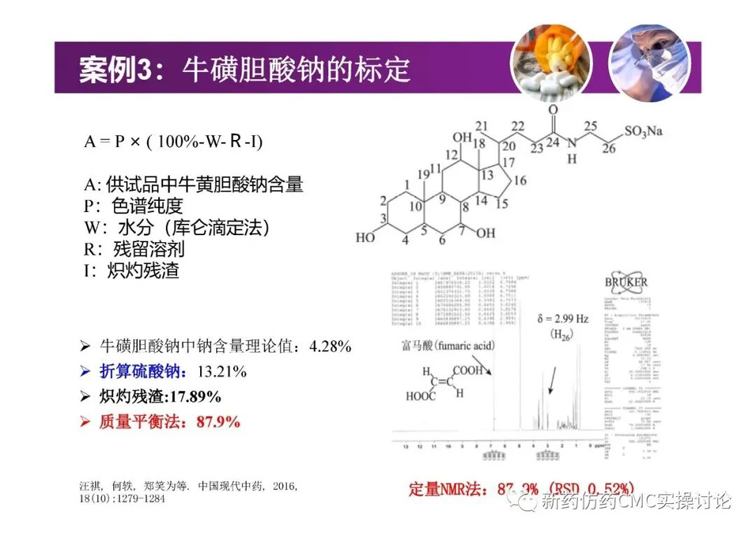
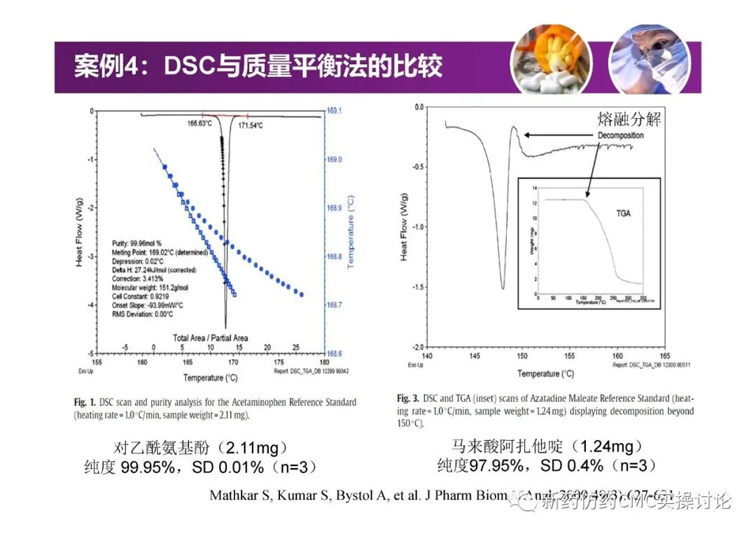
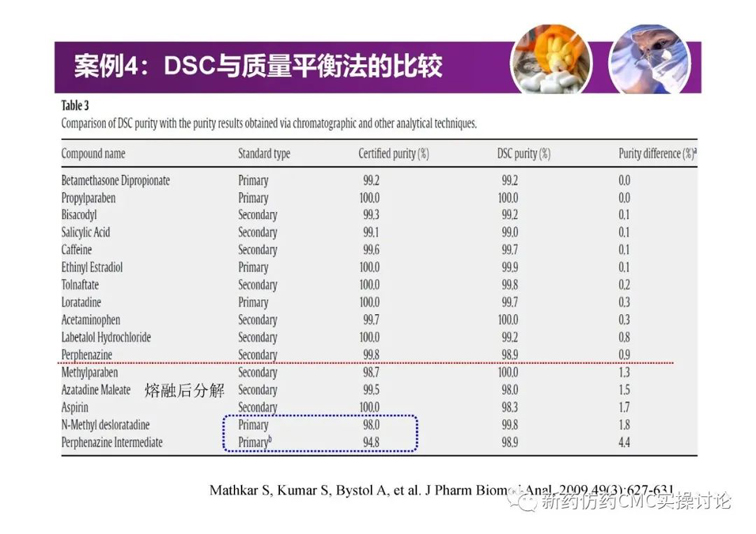
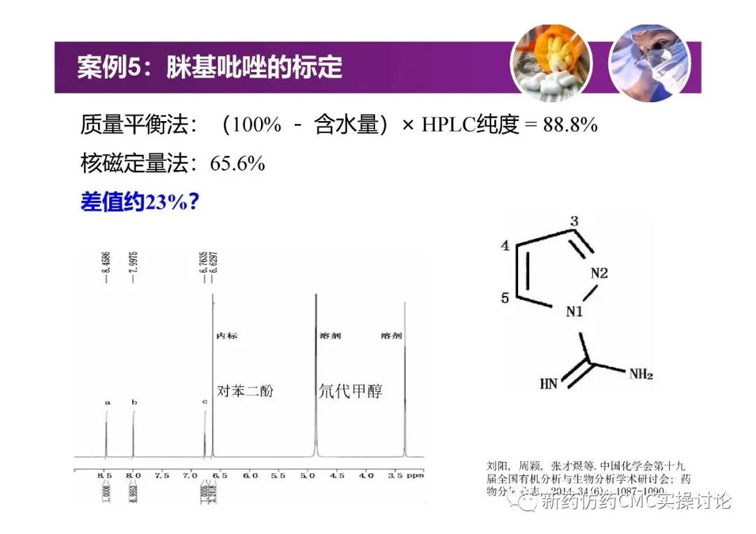
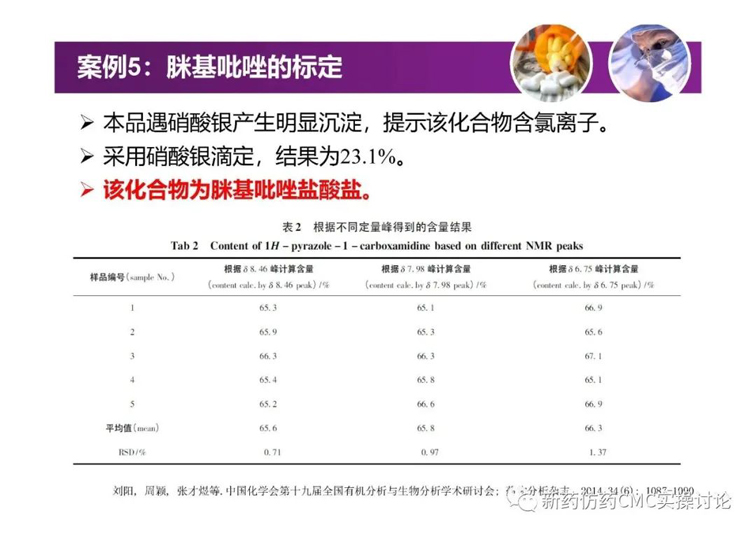
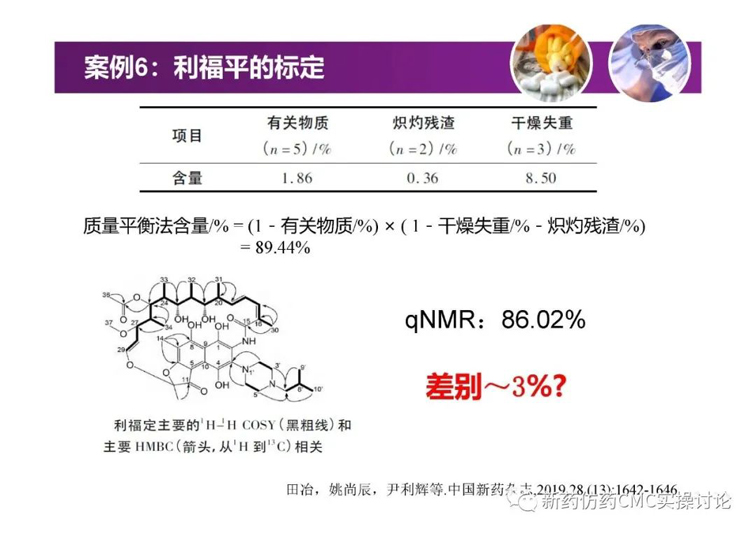
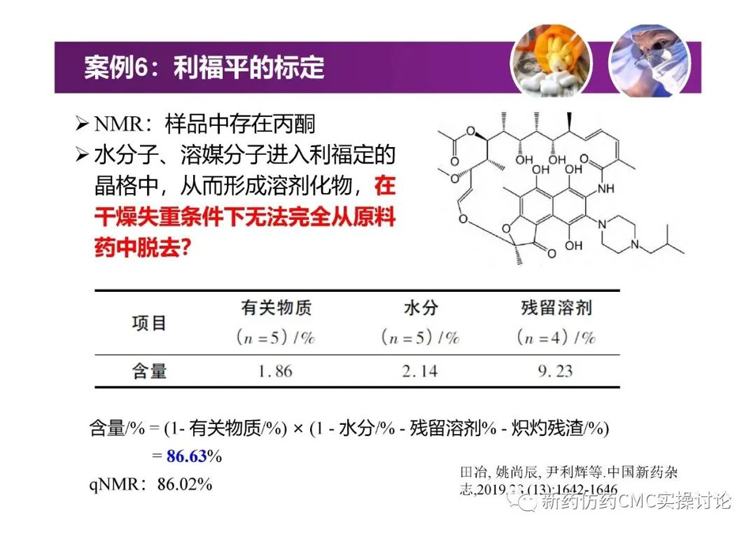
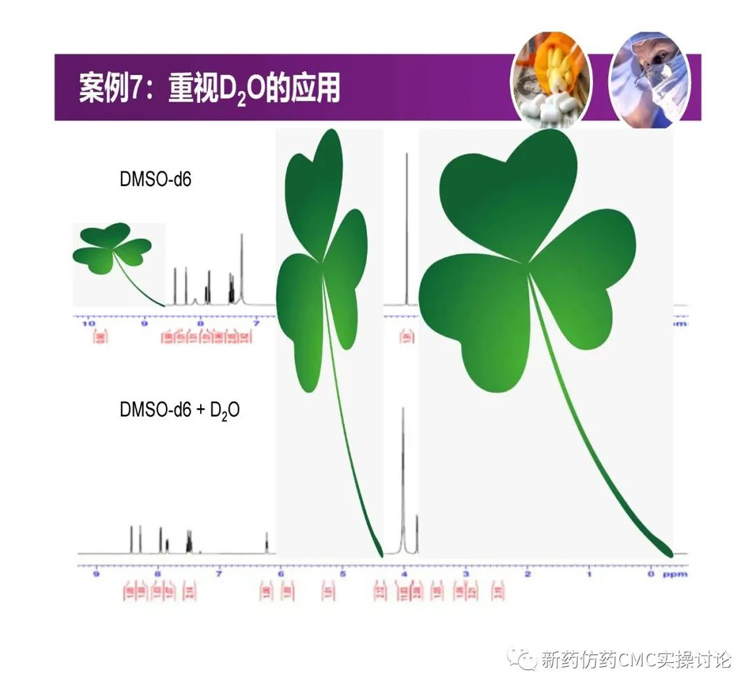
對于吳春勇博士的《化學藥物研發過程中的對照物探討》,新藥仿藥CMC實操討論群也進行了較為熱烈的探討。PPT正文后續延申的討論內容如下(基本按照時間先后順序列出)。
沈曉斌博士(前FDA資深審評員,FDA報批咨詢顧問):
very nice.吳博士論述的非常全面、非常細。我們就說比如說在FDA做review的時候呢,我們個人不會接觸那么全面,各種各樣的方式,這個標準品的這個去就是抽點它的含量呀,就是拿到他的COA,通常不會把各種方法都是看過一遍的。 就是它這個PPT呢,把所有的東西都給想細細的捋了一遍,個人覺得就是這是一個對知識體系的全面的補充,有些東西,因為你以前沒有接觸過,你不會考慮那么細,當在FDA的時候你看到的是公司怎么做,然后你來評估他是否合理,是否可以接受,或者跟FDA的現有要求,來評估。 想要就說一點,FDA本身他不去說去該怎么去定量,這個標準品他只是負責審評,就是評審你(的資料),外界可以自己去建議你想要的方式,但是你要有足夠多的科學依據,然后他(FDA)來評估是否可以接受,就是完全靠自己來論述清楚。 另外就是說國內看起來,這個我以前對國內這個沒有太多的,而且也沒有特別去關注,因為我這個工作最早才從FDA報批方面的東西,吳教授這個主題一講,覺得國內在有些方面其實要求是似乎是比USP、FDA的要求更細更多一些,有一種感覺就是彎道超車已經超了,在有些方面實際上是做的更好。只不過,過去這些年,西方就是設定了這種既定的質量標準,那其他國家,就因為你要照著西方去做仿藥嘛,你就必須根據他的規則來走,更多的是這方面的區別。
孫亞洲老師(長沙晶易首席科學家):
意見1:研發人員買的非法定對照品,外標法測定雜質含量時,很多人直接采用了COA的賦值,也直接采用相應的測定結果訂入了標準,有些不妥。包括批檢驗,最初的朔源需要是法定對照或者經過標定的對照品。
意見2:在吳博士的ppt中,對于非法定來源的如百靈威,sigma等買到的雜質對照品,拿到后是否需要再行進行研究工作或者分析一下是否存在風險,似乎沒有提出來。這個問題建議大家是否深入思考一下。
群主補充:只有經過標化賦值且可溯源(過程,方法,驗證)的,風險才是最低的。
群主補充:盡管雜質測定中,如5%的誤差是可以接受的(這屬于科學性的范疇);但不等同于對照品/標準品可以草率拿來,草率采用他人的賦值,這完全是兩個范疇。也許某份雜質對照品中含水量10%,無機成分包括前處理過程帶來的硅膠等30%,若草率定量,雜質的真實含量會被低估如40%。
沈曉斌博士:同意以上的觀點。
群友1:通過藥品雜質的公司購買的對照品,我們就碰到了,歐美的一家知名公司提供的對照品結構出現偏差,我們通過多次比對都無法拿到和代謝產物吻合的結果,多次交涉和討論之后才發現該公司的產品是另外一個同分異構體。
吳春勇博士(中國藥科大學藥物分析系副教授):看來概率雖然小,這個問題還是客觀存在的。
沈曉斌博士:提供化合物的公司沒有責任和義務。使用者必須做該做的來證明給監管機構標準品的使用是合理的。
劉國柱博士(長沙晨辰醫藥創始人、技術總監):我請教吳博士一個問題,目前國內雜質對照品市場非常混亂,大部分購買的雜質對照品都是經幾手倒賣才到廠家手里,對照品塑源存在問題,譜圖與賦值真實性也存在問題,請問對此引入的風險有何看法?
群友2:在購買對照品的時候,在COA的同時能否得到該合成方法的信息,這個在技術層面上是有難度的。沒有哪個合成公司愿意提供產品合成路線給對方的。
群友3:好多雜質對照品本身不穩定,需要在-20℃保存,有可能在運輸過程中就發生了變化,拿到的第一時間應該進行確認,遇到好幾次這種情況。
吳春勇博士:在現有的條件下,購買的商業化對照品全部自己賦值,實踐上還是存在相當的困難,成本上也沒法控制。所以我個人觀點:
1)盡量選擇知名公司;
2)自己對風險進行評估,尤其是校正因子與各國藥典不同,或者結構上與待測藥物的生色團類似,分子量相當,校正因子卻有顯著不同。 【插話:知名公司依舊有風險或風險大】 是的,分享的那個案例,購買公司是業界相當知名的!
群友4:購買雜質時能同時獲得合成信息的可能性非常小,最多提供四大譜(還不帶解譜的),那就需要公司內部有比較強大的解譜能力,有碰到過解譜結果和供應商提供的不一致的情況,所以購買“商業化”的雜質對照風險是很大,市場良莠不齊,缺乏有效的管控。
群友5:我們碰到問題的那家公司就是業界知名對照品公司,也有出失誤的概率。
劉國柱博士:另請教吳博士及大家一個問題,目前國內許多企業對于雜質對照品的結構確證,很多時候都只做了質譜與NMR氫譜與碳譜,不做二維;而事實上不做二維NMR譜,NMR信號是無法歸屬的,從而不足以確定雜質結構,有可能確證的結構是錯的;請問這個問題大家如何看待?
吳春勇博士:我個人只要做結構確認,一定做二維。
劉國柱博士:那我和您觀點一致,強烈呼吁大家做結構確證一定要做二維。 購買的雜質對照品一般只提供質譜與NMR氫譜與碳譜,不做二維與結構解析;在此習慣引導下,國內許多企業自已做雜質結構確證也只做個質譜與NMR氫譜與碳譜,個人觀點這是存在風險的做法。
代孔恩(安士研發總監):法規有明確規定必須這么表征,很多標準品量很小,做全應該不容易。
【插話:情況多,復雜,沒法一刀切】
黃常康博士(南京百澤醫藥創始人):有些雜質是定向合成的,或者是有文獻數據的。我覺得根據實際情況來判斷需不需要。不用二維定不了結構的,該做就做,有些簡單的雜質,其實氫譜已經足夠了,質譜只是多一個證據。 自己做的話,還需要加上做結構確證的雜質的錢,很多時候會差很多。
群友6:對照品的檢測分析,既要有普遍性的,也要特殊性的,這個普遍性與特殊性的界點怎么界定,很難有一個文件化的說法。
以上討論內容來源: 新藥仿藥CMC實操討論公眾號


