中國科學院過程工程研究所在光控增效型全腫瘤細胞疫苗方面取得新進展
全腫瘤細胞疫苗(whole tumor cell vaccine,TCV)是經典的個體化腫瘤免疫療法,但TCV免疫原性弱且引起的免疫反應個體差異大,亟需通過學科交叉發展新理念和新技術,實現TCV的按需免疫增效。近日,中國科學院過程工程研究所(以下簡稱:過程所)生化工程國家重點實驗室與中國科學院大學化學科學學院合作,創建了新型TCV平臺,依據腫瘤進展情況在接種部位按需實施近紅外光照,以此實現最佳的脈沖免疫增效。相關工作于7月26日發表在Nature Communications(DOI: 10.1038/s41467-023-40207-y)。
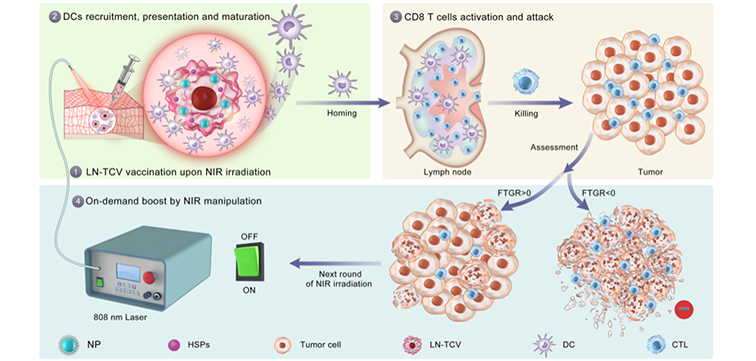
圖1近紅外照射調控全腫瘤細胞疫苗免疫反應的作用機制
腫瘤疫苗通過調動機體免疫系統來對抗腫瘤,是極具前景的腫瘤免疫療法。其中,TCV包含了患者所有潛在的腫瘤抗原,可以通過多價免疫應答減少免疫逃逸,進而實現更加精準的個體化免疫治療。但以往的TCV均需通過經驗式的多次接種來維持免疫反應,患者的腫瘤樣本較為珍貴,使得疫苗的制備和存儲存在較大困難,并且難以針對患者個體充分發揮免疫療效。
面對上述挑戰,過程工程所生化工程國家重點實驗室馬光輝院士和魏煒研究員團隊基于腫瘤免疫治療及生物劑型工程的多年研究基礎,與中國科學院大學化學科學學院田志遠教授展開交叉合作研究。
研究團隊首先發展了新的TCV制備過程,將具有光熱效應的納米顆粒負載于腫瘤細胞中,通過近紅外光照誘導腫瘤細胞產生內源性免疫佐劑熱休克蛋白,反復凍融后形成光控型TCV(LN-TCV)。單次免疫后,近紅外光照誘導接種部位的溫熱反應可產生溫和的炎癥效應,進而招募抗原提呈細胞并促進了后續的抗腫瘤免疫反應。在此基礎上,研究團隊還提出了用于監測腫瘤生長速率波動的新指標(FTGR),以此理性指導在接種部位提供近紅外光照的最佳時機,使得脈沖增效能夠精準契合腫瘤的發展進程。上述LN-TCV在多種細胞來源的腫瘤異種移植模型(CDX)以及人源化的患者來源腫瘤異種移植模型(PDX)中展現出了非常顯著的治療效果,證明了“光控免疫”的新理念在腫瘤疫苗中的先進性和優越性。
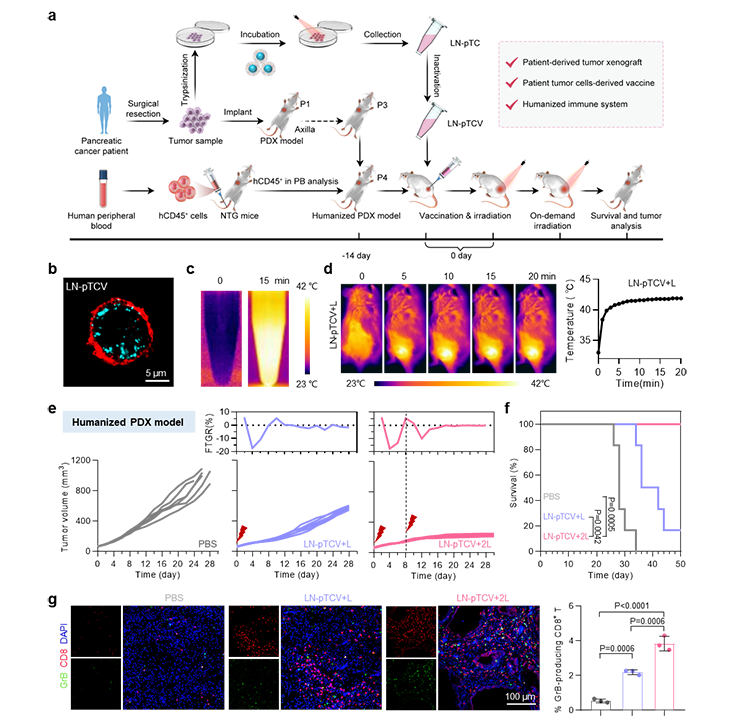
圖2 患者腫瘤細胞來源的LN-pTCV構建及人源化胰腺癌PDX模型的抑瘤實驗:(a)LN-pTCV及人源化胰腺癌PDX模型的構建及免疫策略;(b)LN-pTCV的共聚焦顯微圖像;(c)近紅外光照下LN-pTCV的熱成像圖;(d)近紅外光照下小鼠疫苗接種部位的熱成像圖及溫度變化曲線;(e)PDX模型的抑瘤曲線及相應的FTGR分析;(f)PDX模型的生存曲線;(g)瘤內產生顆粒酶B的CD8 T細胞免疫熒光成像及統計
據研究人員介紹,上述成果仍屬于臨床前研究,實際臨床療效仍有待進一步驗證。鑒于該體系構建的通用性和靈活性,未來轉化研究時以期實現TCV從腫瘤細胞擴展到腫瘤組織的混合細胞,也可以通過可穿戴貼片式LED和遠程控制系統擴展臨床適用場景,實現更加便捷和高效的個體化治療。
近年來,過程工程所生化工程國家重點實驗室馬光輝院士團隊魏煒研究員創制了一系列藥物和疫苗遞送新劑型,在動物模型上成功用于腫瘤、傳染病和炎癥性疾病的防治,并且部分劑型已通過醫院倫理批準進入個體化臨床前和臨床研究。相關工作相繼發表于Nat Nanotechnol 2023, 10.1038/s41565-023-01378-3、Nat Nanotechnol 2021, 16, 1413、Sci Transl Med 2021, 13, eabb6981、Nat Biomed Eng 2023, accepted、Nat Biomed Eng 2021, 5, 414、Nat Biomed Eng 2021, 5, 968、Sci Adv 2021, 7, eabd7614、Sci Adv 2021, 7, eaba2458、Sci Adv 2020, 6, eaay7735、Sci Adv 2019, 5, eaaw3192、Nat Commun 2022, 13, 4214、Nat Commun 2021, 12, 6399、Nat Commun 2019, 10, 5165、Nat Commun 2017, 8, 14537等期刊上。
中國科學院大學博士研究生孟佳琦、過程工程所副研究員呂巖霖、中國科學院大學博士鮑威爾為該論文共同第一作者,過程工程所研究員魏煒、中國科學院院士馬光輝、中國科學院大學教授田志遠為共同通訊作者,中國科學院過程工程研究所為本論文的第一完成單位。該工作得到了國家自然科學基金、北京自然科學基金、國家重點研發計劃和中國科學院戰略性先導科技專項的支持。
論文鏈接:https://www.nature.com/articles/s41467-023-40207-y
生物劑型與生物材料研究部