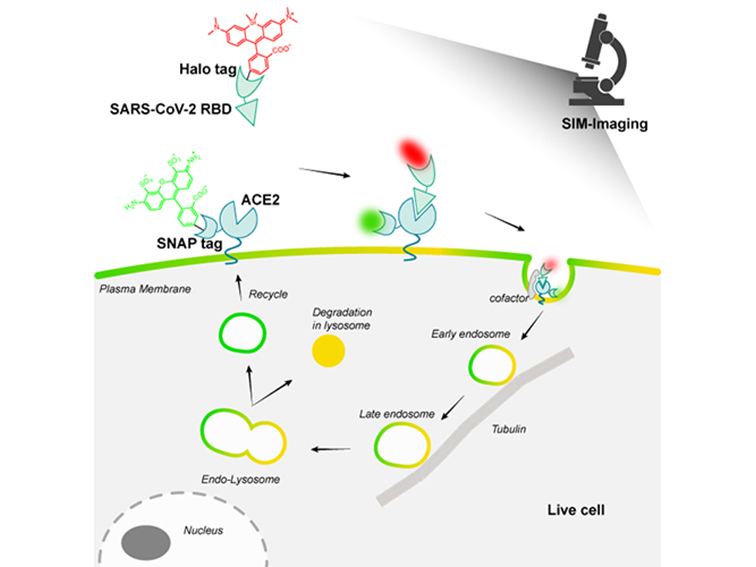
中國科學院大連化學物理研究所解析新冠病毒刺突蛋白RBD細胞內吞過程
近日,中國科學院大連化學物理研究所生物技術研究部分子探針與熒光成像研究組(1818組)徐兆超研究員團隊采用活細胞蛋白定點熒光標記和多色動態超分辨熒光成像的方法,追蹤并分辨出新冠病毒刺突蛋白受體結構域(RBD)進入細胞和胞內降解全過程的多個重要步驟,為新冠病毒致病機理的理解和藥物篩選提供參考和工具。
新冠病毒感染始于病毒的RBD與宿主細胞血管緊張素轉換酶2(ACE2)的結合,之后經歷多階段、多分子的協同作用內吞感染細胞。但這一過程極易受環境干擾,病毒內吞的許多關鍵調控分子和感染細節目前仍然未知。而在活細胞水平上對病毒感染細胞過程的高時空分辨追蹤,能夠全面、真實地揭示病毒的感染機制。
團隊前期發展了活細胞中實時、快速篩選新冠病毒抑制劑的新方法,能夠在1小時內定量檢測被分析物的抑制作用,并最終從2056個化合物中成功篩選出抑制新冠病毒的小分子抑制劑(Acta Pharmaceutica Sinica B,2022)。本工作將Halo和SNAP蛋白標簽分別對RBD和ACE2進行基因編碼,通過標記位點的優化選擇保證了靶蛋白的活性(EC50=25nM)。團隊選擇不同顏色的熒光染料活細胞原位共價連接在蛋白標簽上,從而實現對RBD和ACE2的活細胞標記。借助SIM超分辨成像,團隊追蹤了新冠病毒RBD內吞和細胞內降解的全過程,并發現了多個重要步驟及其細節:RBD與ACE2的結合啟動了內化過程,并形成富含ACE2的囊泡來運輸RBD;隨后,RBD/ACE2囊泡沿微管快速移動,囊泡之間接觸、融合和物質交換,并且在不同微管之間轉移;最后,RBD和ACE2被溶酶體吸收和降解,囊泡中游離ACE2釋放到細胞質中被重新利用。(供稿部門:1818組)
近幾年新冠、甲流和諾如病毒頻發,嚴重影響了人們的生命健康,病毒持續的變異敦促著科研人員對其感染機制開展廣泛而持久的研究。新冠病毒致病機理的超分辨成像研究策略為更多流行病毒的研究打開了新的思路,有助于我們尋求更有效的預防、診斷和治療策略。
相關研究成果以“SIM Imaging Resolves Endocytosis of SARS-CoV-2 Spike RBD in Living Cells”為題,于近日發表在Cell. Chem. Biol.上。該工作的共同第一作者是我所1818組苗露副研究員和博士研究生焉春雨。上述工作得到國家自然科學基金、遼寧省應急攻關項目、我所創新基金等項目的資助。(文/圖 苗露)
文章鏈接: https://doi.org/10.1016/j.chembiol.2023.02.001