中國科學院過程工程研究所在瘤內基因編輯增效ACT療法研究方面取得新進展
過繼T細胞轉移(adoptive T-cell transfer,ACT)療法是極具前景的腫瘤免疫療法,但對實體瘤效果欠佳,亟需通過學科交叉來發展針對實體瘤增效的新理念和新技術。近日,中國科學院過程工程研究所生化工程國家重點實驗室與浙江大學藥學院交叉合作,通過非侵入手段激活實體瘤的基因編輯,并同時調控實體瘤物理和免疫微環境,顯著提升了多種ACT療法對實體瘤的療效。相關工作發表于Nature Nanotechnology(Non-Invasive Activation of Intratumoural Gene Editing for Improved Adoptive T-Cell Therapy in Solid Tumours,DOI: 10.1038/s41565-023-01378-3)。
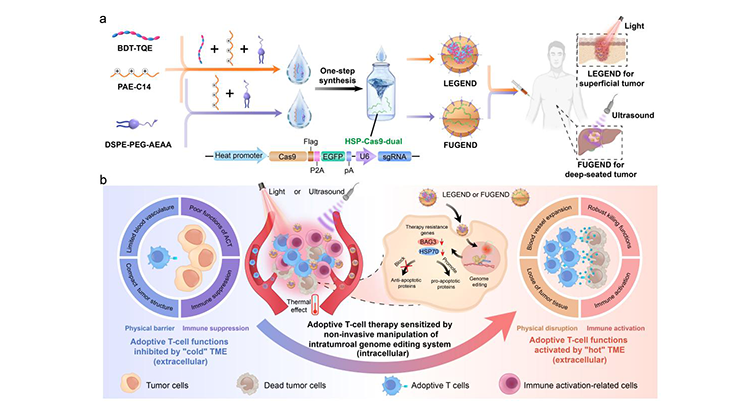
圖1. 光/聲非侵入手段激活瘤內基因編輯增效ACT療法的作用機制
ACT療法通過獲取患者自身T細胞進行體外改造,使其回輸患者體內后識別并攻擊腫瘤細胞。然而,由于實體瘤細胞內的凋亡抗性保護其免于T細胞的殺傷,以及實體瘤細胞外的致密物理屏障、免疫抑制屏障等微環境限制了T細胞向實體瘤深處的浸潤及殺傷功能的發揮,ACT對大多數實體瘤療效不佳。
面對以上諸多挑戰,過程工程所生化工程國家重點實驗室魏煒研究員團隊基于多年腫瘤免疫治療及生物劑型工程研究經驗,與浙江大學藥學院平淵教授團隊展開交叉合作研究。雙方在多維度協同改善細胞內凋亡抗性和細胞外微環境的新理念基礎上,提出利用近紅外光照射(NIR)或聚焦超聲(FUS)非侵入性策略帶來的溫熱效應,激活基因編輯敲除腫瘤細胞抗凋亡基因(HSP70和BAG3),以及打破實體瘤的物理屏障和免疫抑制屏障。通過上述協同作用,在動物腫瘤模型上顯著增強了T細胞的瘤內浸潤和對腫瘤細胞的殺傷效果。
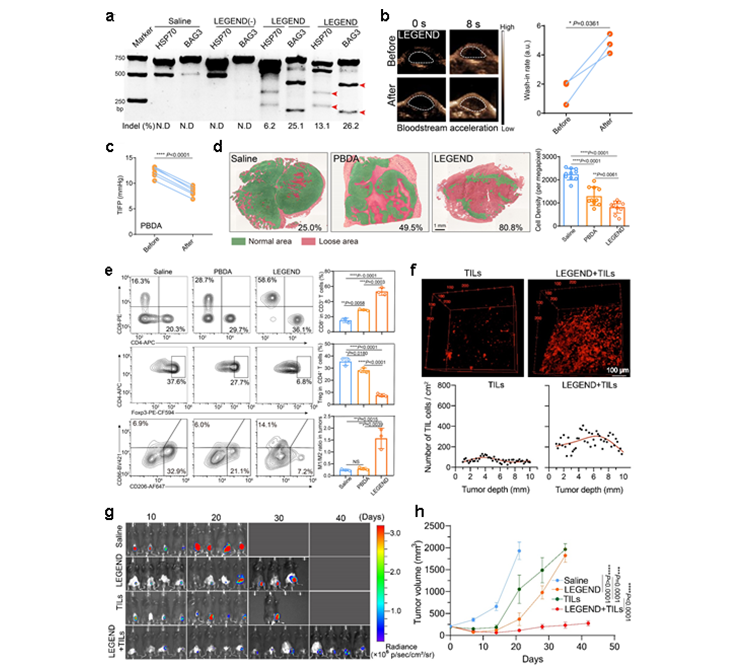
圖2. LEGEND體系多維度協同改善細胞內凋亡抗性和細胞外微環境,提升TIL療法治療效果。a. LEGEND+NIR照射激活瘤內基因編輯,敲除腫瘤細胞抗凋亡基因(HSP70和BAG3);b-d. NIR溫熱效應打破實體瘤的物理屏障,包括血流加速(b)、間質壓力降低(c)、組織疏松(d);e. NIR溫熱效應改善腫瘤免疫抑制微環境;f. LEGEND處理后顯著增強TIL的瘤內浸潤;g-h. LEGEND處理后顯著提升TIL回輸療法的抑瘤效果。
其中,針對淺表腫瘤,研究團隊發展了光驅動型基因編輯納米器件(LEGEND),采用“納米器件瘤周注射+NIR照射”的方式,在黑色素瘤等小鼠腫瘤模型以及人源化的患者來源腫瘤異種移植模型上顯著提升了腫瘤浸潤T細胞和嵌合抗原受體T細胞兩種過繼回輸T細胞療法的治療效果。針對深部腔內腫瘤,研究團隊進一步發展了聚焦超聲驅動型基因編輯納米器件(FUGEND),采用“納米器件靜脈注射+FUS”的方式,在小鼠原位肝癌模型上同樣證明了顯著的ACT增效作用。
據研究人員介紹,上述成果仍屬于臨床前研究,實際臨床療效仍有待進一步驗證。鑒于該體系構建的通用性和靈活性,未來臨床轉化時可以按照不同治療需求采用不同的基因編輯策略及非侵入操控方式。
近五年來,過程工程所生化工程國家重點實驗室馬光輝院士團隊魏煒研究員創制了一系列藥物和疫苗遞送新劑型,在動物模型上成功用于腫瘤、傳染病、炎癥性疾病的防治,并且部分劑型已通過醫院倫理批準進入個體化臨床前和臨床研究。相關工作相繼發表于Nat Nanotechnol 2021, 16, 1413、Sci Transl Med 2021, 13, eabb6981、Nat Biomed Eng 2023, accepted、Nat Biomed Eng 2021, 5, 414、Nat Biomed Eng 2021, 5, 968、Sci Adv 2021, 7, eabd7614、Sci Adv 2021, 7, eaba2458、Sci Adv 2020, 6, eaay7735、Sci Adv 2019, 5, eaaw3192、Nat Commun 2022, 13, 4214、Nat Commun 2021, 12, 6399、Nat Commun 2019, 10, 5165、Nat Commun 2017, 8, 14537等期刊上。
浙江大學藥學院陳小紅博士、過程工程所王雙副研究員、浙江大學藥學院博士生陳宇軒為該論文共同第一作者,浙江大學藥學院平淵教授、過程工程所魏煒研究員為共同通訊作者。該工作得到了國家重點研發計劃項目、國家自然科學基金項目和浙江省自然科學基金的支持。
論文鏈接:https://www.nature.com/articles/s41565-023-01378-3
生物劑型與生物材料研究部